Extracción de antioxidantes de los arándanos (Vaccinium corymbosum): efecto de solventes verdes sobre polifenoles totales, capacidad antioxidante y comportamiento electroquímico
Extraction of Antioxidants from Blueberries (Vaccinium Corymbosum): Effect of Green Solvents on Total Phenolic Content, Antioxidant Capacity and Electrochemical Behavior
Recibido: 15 diciembre 2021
Aceptado: 3 mayo 2022
Disponible: 1 junio 2022
J. F. Bedoya-Cataño; C. Ramón-Palacio; M. A. Gil-Garzón; C. Ramírez-Sánchez, “Extracción de antioxidantes de los arándanos (Vaccinium Corymbosum): efecto de solventes verdes sobre polifenoles totales, capacidad antioxidante y comportamiento electroquímico” TecnoLógicas, vol. 25, nro. 53, e2277, 2022. https://doi.org/10.22430/22565337.2277
Highlights
Resumen
El presente estudio tuvo como objetivo evaluar el efecto de solventes verdes como el etanol/agua (EtOH/H2O), ácido acético/agua (CH3COOH/H2O) y la mezcla etanol/ácido acético/agua (EtOH/CH3COOH/H2O) en la extracción de polifenoles, específicamente antocianinas, provenientes de la especie Vaccinium corymbosum, con el fin de determinar su capacidad antioxidante mediante el comportamiento electroquímico. Para los extractos obtenidos se determinó el contenido de antocianinas totales (CAT) y contenido de polifenoles totales (CPT) por medio de técnicas espectrofotométricas y la capacidad antioxidante (CA) mediante el comportamiento electroquímico determinado a través de voltamperometría cíclica. Los resultados obtenidos indican que, si bien cuando se tiene EtOH/H2O como solvente se alcanza una mayor extracción de polifenoles, (696.46 ± 26.55) mg equivalente de ácido Gálico/100 g de muestra de base húmeda (bh), con la mezcla de solventes EtOH/CH3COOH/H2O se logra una mayor extracción de antocianinas (82.09 ± 2.59) mg equivalentes de cianidina-3-glucósido/100 g bh de muestra, lo cual concuerda con la capacidad antioxidante por voltamperometría cíclica, donde el mayor valor se obtuvo para la mezcla EtOH/CH3COOH/H2O (270.96 ± 10.74) µmol equivalente de ácido gálico/g bh de muestra), es decir que mayor concentración de antocianinas monoméricas dentro del contenido de polifenoles totales fueron oxidadas en el electrodo de trabajo. En este orden de ideas, se puede concluir que existen diferencias significativas entre el efecto que tuvo la evaluación de los solventes en el método de extracción sobre cada uno de los valores promedios alcanzados para los aspectos evaluados (CPT, CAT y CA), con una confianza del 95 %. Además, hay una “fuerte” correlación positiva entre el CAT y la capacidad antioxidante (r = 0.95).
Palabras clave: Actividad antioxidante, análisis electroquímico, antocianinas, solventes verdes, Vaccinium corymbosum.
Abstract
In this study the effect of green solvents such as ethanol/water (EtOH/H2O), acetic acid/water (CH3COOH/H2O), and ethanol/acetic acid/water (EtOH/CH3COOH/H2O) was evaluated on polyphenols extraction, specifically anthocyanins that come from Vaccinium corymbosum specie, to determine its antioxidant capacity using electrochemical behavior. Total anthocyanin content (CAT) and total polyphenols content (CPT) were determined in the extracts employing spectrophotometric techniques and antioxidant capacity (CA) through electrochemical behavior using cyclic voltammetry. When EtOH/H2O is used as a solvent system, a higher polyphenols extraction is achieved, (696.46 ± 26.55) mg equivalent of gallic acid /100 g in fresh basis sample (bh), with EtOH/CH3COOH/H2O solvent mixture, more content of anthocyanins was extracted, (82.09 ± 2.59) mg equivalent of cyaniding-3-glucoside/ 100 gbh of sample, which agrees with the antioxidant capacity by cyclic voltammetry, where the highest value was obtained for the EtOH/CH3COOH/H2O mixture (270.96 ± 10.74) µmol equivalent of gallic acid /100 gbh of sample), i.e., higher concentration of monomeric anthocyanins within the total polyphenol content were oxidized at the working electrode. There are significant differences between the effect of solvent evaluation in the extraction method on each average value achieved in evaluating aspects (CPT, CAT, and CA) with a confidence level of 95 %. Additionally, there is a “strong” positive correlation between CAT and antioxidant capacity (r = 0.95).
Keywords: Antioxidant activity, Electrochemical analysis, Anthocyanins, Green Solvents, Vaccinium corymbosum.
1. INTRODUCCIÓN
Los arándanos son frutos conocidos por sus beneficios para la salud, alto valor nutricional y una buena evaluación sensorial [
Los derivados polifenólicos se clasifican en dos principales grupos: flavonoides (isoflavonoides, antocianidinas, flavanoles, flavonoles, flavanonas y flavonas), presentes con mayor frecuencia en recursos naturales como las frutas, hortalizas y otros alimentos [
Los arándanos contienen principalmente flavonoles como la quercetina y derivados, antocianinas, flavan-3-ol y proantocianidinas. Adicionalmente, contiene no flavonoides como los ácidos benzoico e hidroxicinámico y sus derivados como ácidos gálico, caféico, clorogénico, p-coumarico, ferúlico y vanílico [
La capacidad antioxidante de los arándanos se ha evaluado mediante alternativas analíticas que se agrupan según su fenómeno de reacción, destacando así los ensayos basados en fenómenos de radicales libres, DPPH´ (2,2 difenil-1-picrilhidrazilo) y ABTS´+ (ácido 2,2'-azino-bis-3etilbenzotiazolina-6-sulfónico), ensayos que tienen como principio la reducción de iones metálicos, FRAP (Poder de Reducción Antioxidante de ion Férrico), Folin Ciocalteu (reducción de sales de molibdeno y wolframio), CUPRAC (Capacidad Antioxidante Reductora Cúprica), el método ORAC (capacidad de absorción de radicales de oxígeno), son los más comunes [
Adicional a los estudios usados anteriormente, hay un auge en las técnicas electroquímicas para la caracterización de especies electroactivas, permitiendo evaluar su capacidad antioxidante y favorecer el reconocimiento de modelos de comportamiento y fenómenos de transferencia de electrones, empleados en la identificación de matrices de gran complejidad [
Para la determinación de la capacidad antioxidante, un factor importante es la técnica de extracción de los polifenoles, entre las cuales se encuentra la extracción por solventes, la cual es una técnica ampliamente conocida y tiene como ventaja que se puede reproducir fácilmente a escala industrial. Los solventes más utilizados para la extracción de antioxidantes de los frutos rojos en general, han sido metanol [
En la búsqueda de procesos amigables con el medioambiente, el uso de solventes verdes se convierte en una parte importante en la extracción de polifenoles para un acercamiento a procesos más limpios en consonancia con los Objetivos de Desarrollo Sostenible [
Aunque los arándanos se han abordado ampliamente en la literatura, hacen falta estudios en los que se evalúe el efecto de solventes verdes en la extracción de polifenoles. Por esto, este trabajo tiene como objetivo evaluar el efecto de solventes verdes como el etanol/agua (EtOH/H2O), ácido acético/agua (CH3COOH/H2O) y la mezcla etanol/ácido acético/agua (EtOH/CH3COOH/H2O) para la extracción de polifenoles, específicamente antocianinas provenientes de la especie Vaccinium corymbosum, con el fin de determinar su capacidad antioxidante mediante el comportamiento electroquímico.
2. METODOLOGÍA
2.1. Reactivos
Para el desarrollo experimental, se empleó Etanol comercial (EtOH) al 70 %, Ácido acético comercial (CH3COOH) al 5 %, Agua desionizada, reactivo Folin Ciocalteu (Merk), Ácido gálico (Merk), Buffer acetato de sodio/ácido acético pH 4.5 (0.995 M) y pH 3.0 (0,1 M), Buffer de cloruro de potasio ajustado con HCl pH 1.0 (0.0625 M), hipoclorito de sodio comercial (NaClO) al 5.25 %, y Ácido nítrico HNO3 (0.1 M).
2.2. Preparación preliminar de la muestra
Se obtuvieron tres unidades experimentales independientes de arándano Vaccinium corymbosum de marca comercial (Fructífera S.A.S, Cundinamarca-Colombia). Las muestras se desinfectaron con hipoclorito de sodio, NaClO al 5.25 % y se dejaron secar durante 12 horas a temperatura ambiente. Luego, se secaron a 40 °C durante 30 h. Finalmente, se redujo el tamaño del fruto completo (pulpa y cáscara) y se pasaron por un tamiz de 1 mm.
2.3. Obtención de extractos
El proceso de extracción del arándano Vaccinium corymbosum, se realizó a través de la inmersión en tres sistemas de solventes. El primero, consistió en la mezcla (1:1) de etanol y agua (EtOH/H2O). La segunda, conformada por ácido acético y agua (CH3COOH/H2O) en relación (1:1). Por último, una mezcla de etanol, ácido acético y agua (EtOH/CH3COOH/H20), en relación (1:1:1).
Para la extracción, se tomaron 1.5 g del fruto en polvo de cada unidad experimental a los cuales le añadió un volumen de 30 mL de la mezcla de solvente a evaluar, alcanzando así una concentración de 0.05 gmuestra /mLsolvente, se dejó en contacto durante 68 h, protegidas de la luz, manteniendo agitación mecánica cada 6 h durante 1 min. Finalmente, se filtró, se extrajo el sobrenadante y se conservó en congelación hasta el análisis químico. Este procedimiento se realizó con cada sistema de solvente evaluado y por triplicado.
2.4. Determinación del Contenido de Antocianinas Totales (CAT)
Para cuantificar el contenido de antocianinas totales del arándano Vaccinium corymbosum, se llevó a cabo el método de pH diferencial [
Finalmente, la concentración total de antocianinas monoméricas (AT) se expresó en términos de miligramo equivalente de cianidina-3-glucosido, mg C3G/100 g de Fruto Fresco (FF), de acuerdo a la ecuación (1) [
Donde ∆A (antocianinas totales)=(A máx 510nm-A 700nm)pH1.0-(A máx 510nm-A 700nm) pH 4.5, PM (peso molecular de la cianidina-3-glucosido, 449.2 g/mol), FD (factor de dilución), y ε (coeficiente de extinción molar, 26900 L/mol.cm).
2.5 Determinación del Contenido de Polifenoles Totales (CPT)
Para cuantificar el contenido de compuestos fenólicos del extracto de arándano se realizó por el método de Folin Ciocalteu. Para ello, se preparó una curva de calibración de ácido gálico de 10, 20, 40, 60, 80 y 100 μg/mL con R2 de 0.9937.
Con el extracto de Vaccinium corymbosum se prepararon diluciones de las 3 muestras de solventes en relación 1:100. Además, se adicionó en recipientes 2250 μL de agua destilada, 450 μL de agua destilada adicional para el blanco, 300 μL de la muestra, 300 μL de Na2CO3 al 10 % y 150 μL del reactivo de Folin a 25 °C incubando durante 60 minutos en completa oscuridad. Luego, se midió la absorbancia en un espectrofotómetro Agilent 8453 UV-Visible a 760 nm realizando las mediciones por triplicado.
Finalmente, se expresa la concentración total de antioxidantes en equivalentes en miligramos de ácido gálico por cada cien gramos de fruto fresco (FF) (mg EAG/100 g FF) según (2) [
2.6 Determinación de la Capacidad Antioxidante (CA)
2.6.1 Método voltamperometría cíclica (CV)
Para evaluar la capacidad antioxidante de los extractos del arándano Vaccinium corymbosum, se desarrolló a través del método electroquímico de voltamperometría cíclica (CV). Se utilizó un potenciostato PSTrace Sensit Smart y una configuración de celda de tres electrodos: electrodo de trabajo de Au de 3 mm de diámetro, un contraelectrodo de grafito y un electrodo de referencia de Calomel en KCl 3 M.
Como pretratamiento, se pulió la superficie del electrodo de trabajo con polvo de alúmina de 3 μm y se lavó con alcohol etílico al 70 % por ultrasonido durante 5 min [
Se realizó una curva de calibración de ácido gálico con soluciones en 0.1, 0.3, 0.5, 0.8 y 1.0 mM por voltamperometría cíclica usando 1 mL de solución de ácido gálico y 10 mL de una solución buffer de acetato de sodio/ácido acético 0.1 M a pH 3.0. Se realizaron barridos de potencial de 0 a 1.0 V y una velocidad 10 mV/s.
Para los extractos de arándanos, se tomaron alícuotas de 200 μL y 10 ml de electrolito soporte, se realizó la voltamperometría cíclica por triplicado y se expresaron los resultados en equivalentes en µmol de ácido gálico por gramos de fruto fresco (µmol EAG/g FF) según (3).
2.7 Evaluación de riesgo de los solventes
Con el propósito de evaluar el nivel de riesgo de cada uno de los solventes empleados, se desarrolló a través de la metodología propuesta por [
Esta guía propuesta por sociedad europea promotora de metodologías biológicas y químicas sostenibles relaciona un conjunto de criterios de seguridad, salud y medio ambiente en base a referencias de las guías existentes que están alineados con el Sistema Globalmente Armonizado y la normativa europea [
Adicionalmente, se complementó de acuerdo a la introducción del concepto de extracción verde en los procesos de obtención de compuestos naturales y la importancia de la aplicación de análisis de ciclos de vida, además de la orientación de las propuestas verdes con respecto el empleo de solventes [
2.8 Análisis estadístico
La evaluación de las diferencias entre los tres sistemas de solventes se llevó a cabo mediante un Análisis de Varianza, ANOVA donde la variable respuesta fue el contenido total de polifenoles (CPT), contenido de antocianinas totales (CAT) y capacidad antioxidante (CA).
Se empleó una prueba de Tukey para determinar si existían diferencias entre los tratamientos evaluados por pares, con una significancia P-valor<0.05 mediante el software RStudio. Los datos fueron presentados como el promedio y la desviación estándar. Tres muestras (n=3) de cada unidad comercial fue analizada y todos los análisis fueron presentados por triplicado.
Además, se evaluó la matriz de correlaciones (r) y regresión lineal (R2) entre la capacidad antioxidante asociada al contenido de polifenoles y antocianinas totales, para medir la relación entre pares de variables, a través de la herramienta de análisis de Microsoft Excel® con F-valor calculado > F crítico.
En la Figura 1 se presenta un esquema resumen del desarrollo metodológico empleado.

3. RESULTADOS Y ANÁLISIS
3.1 Determinación del contenido de polifenoles y antocianinas totales
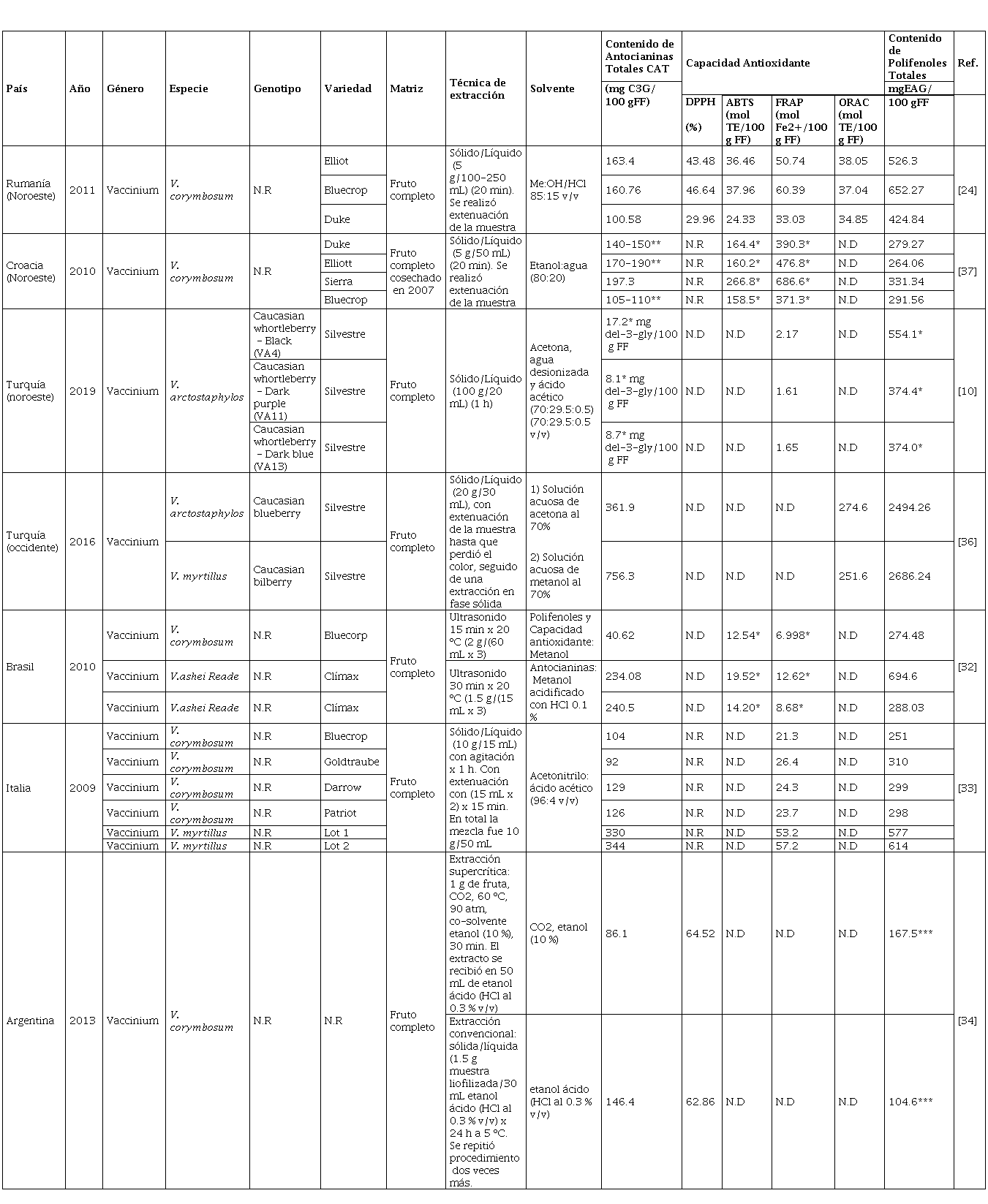
La caracterización del contenido de polifenoles totales en el proceso de extracción de antioxidantes de pulpa y cáscara de arándano Vaccinium corymbosum, se presenta en la Tabla 1.
obtenido con etanol (EtOH/H2O), ácido acético (CH3COOH/H2O) y etanol ácido
acético (EtOH/CH3COOH/H2O). Fuente: elaboración propia.
| Tratamiento | Contenido de Polifenoles Totales, CPT | Contenido de Antocianinas Totales, CAT | CAT/CPT | ||
| (mg EAG/100 g FF)1 | Coeficiente Variación, % | (mg C3G/100 g FF)2 | Coeficiente de Variación, % | ||
| EtOH/H2O | 696.46 ± 26.55a | 3.81 % | 26.95 ± 4.36a | 16.17 | 3.87 % |
| CH3COOH/H2O | 630.09 ± 39.82ab | 6.32 % | 63.59 ± 11.19b | 17.59 | 10.09 % |
| EtOH/CH3COOH/H2O | 543.07 ± 48.74b | 8.97 % | 82.09 ± 2.59b | 3.16 | 15.12 % |
Los valores están expresados en base húmeda o fruto fresco (FF) y reportados como valor medio
y desviación estándar (SD), n = 3. Las letras superíndice diferentes en la misma columna,
indican diferencias significativas (p < 0.05 por la prueba de Tukey).
1 Resultados expresados como EAG (equivalente a ácido gálico).
2 Resultados expresados como equivalentes a cianidin-3-glucosido.
Los resultados del CPT y CAT permiten evidenciar, como la variación del sistema de solventes empleados tienen una efectividad que difieren estadísticamente. Desde el punto de vista del contenido de compuestos funcionales presentes en el extracto de arándanos, se identificó que los valores promedios del CPT obtenidos mediante la extracción realizada con EtOH/H2O difieren significativamente de la realizada con la mezcla de EtOH/CH3COOH/H2O, siendo superior la capacidad de extracción del sistema binario de solventes próticos en un 22 %, debido probablemente a las características de polaridad de ambos solventes, ya que el agua es el solvente más polar conocido, sumado a la capacidad de penetración y solvatación que se logra con el balance que aporta el etanol, al tener una densidad menor que el agua (detanol=0.789 g/mL, dagua=1.000 g/mL). Por otra parte, se ha relacionado que la capacidad de extracción de compuestos polares, como los polifenoles puede favorecerse en presencia de solventes con un alta constante dieléctrica, pero que tiene como limitante la temperatura, ya que este comportamiento puede darse de forma óptima a bajas temperaturas y, por el contrario, afectar la estabilidad de algunos compuestos fenólicos termolábiles, al aumentarla.
Por esta razón, se proyectó una mezcla que tuviera un balance en cuanto el aporte de la constante dieléctrica con ambos solventes (ketanol=24.625ºC, kagua=77.4625ºC) a la temperatura de análisis (18 ºC), de manera que conservara la capacidad para disminuir la energía intermolecular y mantener aún niveles altos de polaridad. Esta propiedad, pudo verse afectada de manera negativa en la mezcla EtOH/CH3COOH/H2O, considerando que esta relación en presencia del CH3COOH, el cual posee la kacético=6.225ºC [
En contraste, el análisis del CAT muestra un comportamiento diferente al que se presentó con el CPT, ya que el mayor contenido de antocianinas monoméricas se alcanzó justo con el sistema EtOH/CH3COOH/H2O y, por el contrario, el menor contenido se relaciona al tratamiento de extracción con EtOH/H2O, lo que conllevó a que este último difiriera significativamente del promedio reportado para los dos CAT reportados para ambos sistemas en presencia de CH3COOH, como se muestra en la Figura 2.
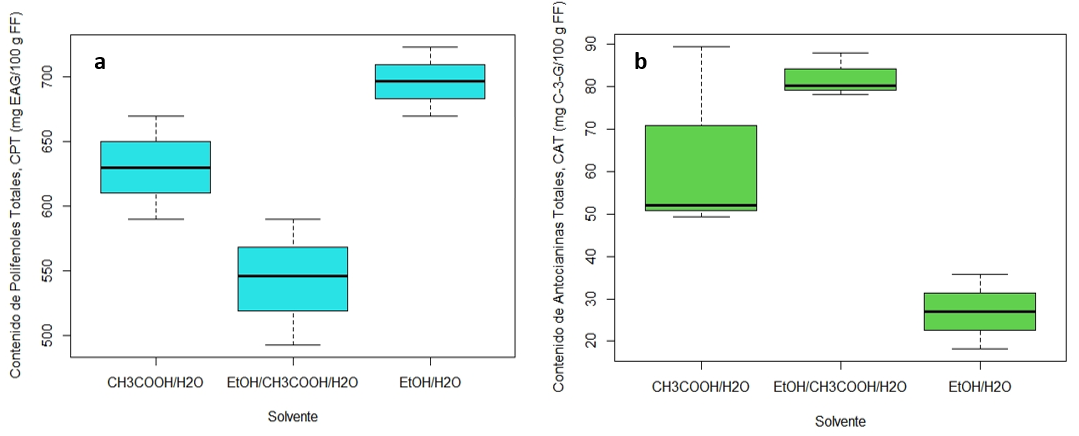
El comportamiento diferente en la capacidad de extracción de las antocianinas con cada uno de los sistemas de solventes evaluados, puede deberse a la estabilidad de las antocianinas a bajos pH [
* Los valores se ajustaron a las unidades de mg/100 g
** Se reporta un rango aproximado, ya que los autores representan gráficamente los valores sin que haya una precisión en la graduación de la escala de valores de contenido de antocianinas totales
NR: No Reportado
N.D. No Determinado del-3-gly: delphinidin-3-glucoside
*** Valor reportado en base seca
Sumado a lo anterior, desde el punto de vista del solvente prótico empleado, se identificó que en los estudios analizados, el mayor valor reportado (756.3 mg C3G/100 g FF), lo reportan en Turquía [
En complemento, este estudio de máximo rendimiento [
De acuerdo a la literatura, el contenido de antocianinas totales dentro del grupo de bayas puede variar significativamente entre 10 a 600 mg C-3-G/100 g Fruto Fresco, que dependerá de la especie, su variedad, su tamaño, estado de maduración, y de las condiciones ambientales [
La relación CAT/CPT para el tratamiento EtOH/CH3COOH/H2O alcanzó un valor de 0.15, igual al reportado por [
De acuerdo con el análisis de regresión, se logra mostrar como la relación entre el CAT y CPT de los tratamientos evaluados tienen una tendencia inversamente proporcional, como se muestra en la Figura 3, explicado por un coeficiente de determinación de 93.13 %. Este comportamiento es resultante, en consecuencia, de la mayor efectividad de extracción del contenido de polifenoles totales con el solvente prótico EtOH/H2O, no solo para la obtención de antocianinas, sino también los demás compuestos fenólicos en la muestra, que consiste en flavonoides y flavan-3-ol [
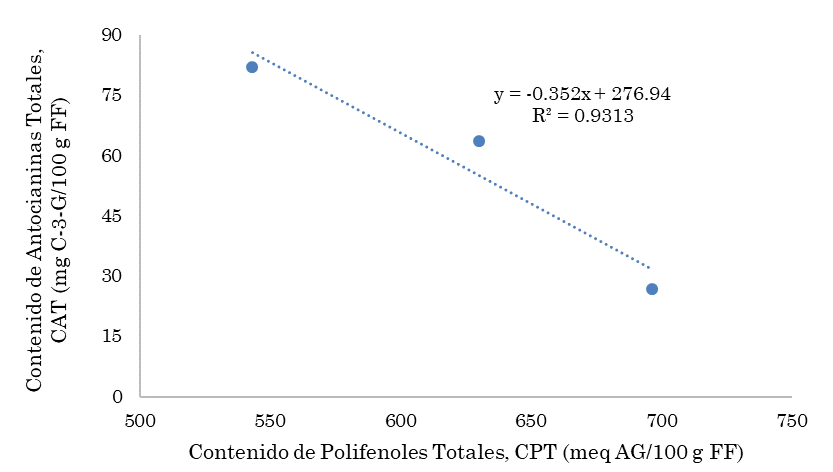
Finalmente, el análisis de correlación realizado para ambas variables muestra un r = 0.9659 (valor Fcalculado (13.55) > Fcrítico (0.17)), indicando que esta relación es “alta” o “fuerte”, a pesar de tener una tendencia inversa.
3.2 Determinación de capacidad antioxidante por un método electroquímico
En la Figura 4 se presentan los voltamperogramas y curva de calibración obtenidos para 5 concentraciones diferentes de ácido gálico. Es posible observar principalmente dos picos de oxidación a 0.40 V y 0.90 V, los cuales son ausentes para la primera curva correspondiente al blanco (buffer de acetatos), mostrando que ambos picos pertenecen a la oxidación del ácido gálico. El primer pico corresponde a la oxidación del grupo OH que se encuentra en posición para al ácido carboxílico, mientras que el segundo pico pertenece a la oxidación de un grupo OH en posición meta [5]. Para la realización de la curva de calibración se tomó la corriente en el segundo pico, en dirección anódica.
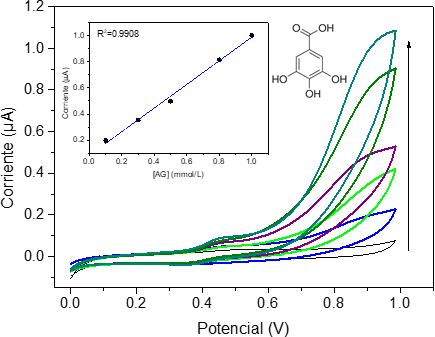
Para evaluar el comportamiento electroquímico de los extractos de arándanos, se realizaron voltamperometrías cíclicas para las muestras obtenidas por los tres solventes diferentes: EtOH/H2O, CH3COOH/H2O y EtOH/CH3COOH/H2O. Las CV fueron barridas desde 0 a 1.0 V a una velocidad de 10 mV/s, las cuales son registradas en la Figura 5. Para los tres sistemas de solventes se presentan 2 picos alrededor de 0.40 V y 0.90 V, mostrando la oxidación de compuestos electroquímicamente activos dentro de los extractos.
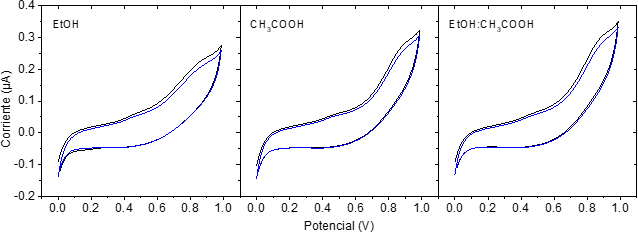
El análisis de los potenciales de oxidación puede dar información de la fuerza del polifenol como agente reductor, entre menor sea el potencial de oxidación, más fácilmente se oxida la molécula y dona electrones [
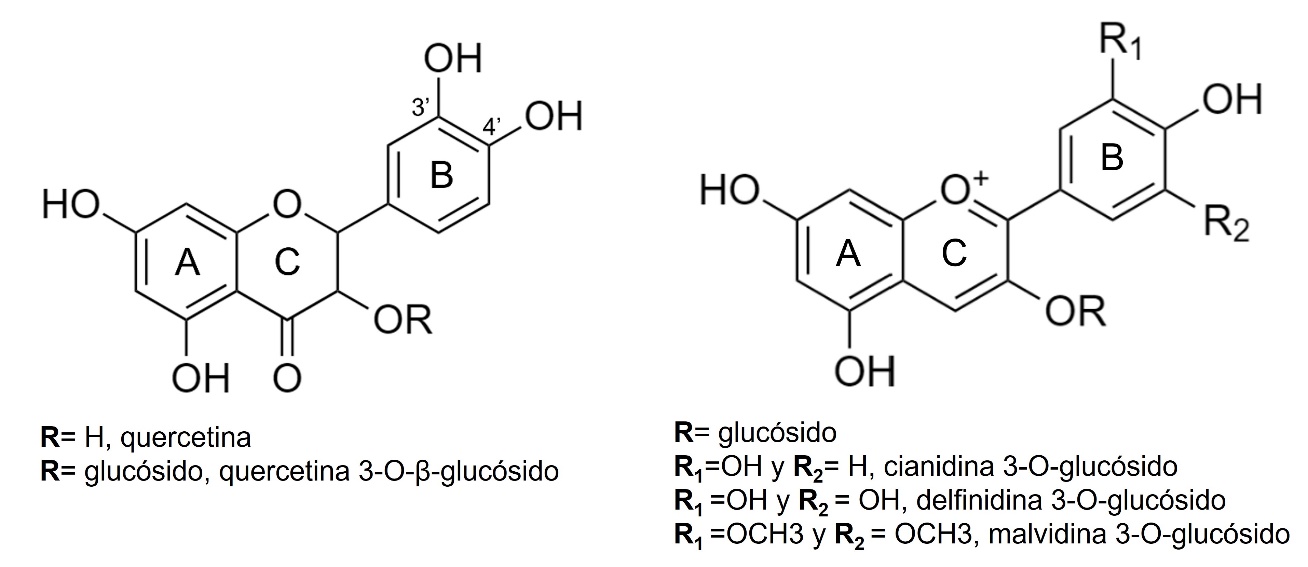
Estudios voltamperométricos previos realizados en arándanos, Nikolić y colaboradores (2019), atribuyen el primer pico anódico a la oxidación de moléculas como quercetina y quercetina 3-O-glucósido presentadas en la Figura 6a, donde reaccionan los grupos hidroxilo sustituyentes 3’ y 4’ del anillo B [
Aunque el comportamiento electroquímico de los compuestos electroactivos en los sistemas de solventes evaluados es similar, es posible observarse algunas diferencias en el pico alrededor de 0.90 V, el cual la magnitud de la corriente alcanzada se da en el orden EtOH/H2O < CH3COOH/H2O < EtOH/CH3COOH/H2O. Es importante tener en cuenta que la magnitud de la corriente es proporcional a la concentración de antioxidantes presentes en la muestra [
En la Tabla 3 se reporta el equivalente de ácido gálico para los tres extractos, usando la curva de calibración presentada en la Figura 4 y las densidades de corrientes obtenidas en el segundo pico de oxidación, alrededor de 0.90 V. Los resultados se expresaron como los promedios ± la desviación estándar del análisis por triplicado.
arándano Vaccinium corymbosum en etanol (EtOH/H2O), ácido acético (CH3COOH/H2O) y etanol
ácido acético (EtOH/CH3COOH/H2O). Fuente: elaboración propia.
| Capacidad Antioxidante Total, CA | ||
| Tratamiento | µmol EAG/g FF1 | Coeficiente de Variación, CV (%) |
| EtOH/H2O | 204.77 ± 4.29a | 2.10 % |
| CH3COOH/H2O | 230.97 ± 16.59a | 7.18 % |
| EtOH/CH3COOH/H2O | 270.96 ± 10.74b | 3.96 % |
Los valores están expresados en base húmeda o fruto fresco (FF) y reportados como valor medio y desviación
estándar (SD), n = 3. Las letras superíndice diferentes en la misma columna, indican diferencias significativas
(p < 0.05 por la prueba de Tukey). 1 Resultado expresado como EAG (equivalente a ácido gálico).
La capacidad antioxidante medida por CV usando un equivalente en ácido gálico, muestra que la mezcla EtOH/CH3COOH/H2O puede extraer mayor contenido de polifenoles y por lo tanto presenta mayor capacidad antioxidante. Es importante observar que esta misma mezcla arroja mayor contenido de antocianinas como se mostró en la Tabla 1, este comportamiento puede deberse a que, para hallar la capacidad antioxidante de los sistemas por CV, se usó la corriente del segundo pico el cual se relaciona con la oxidación de los grupos OH de las antocianinas.
Las antocianinas existen en diferentes configuraciones estructurales dentro de la naturaleza, ya sea protonadas, desprotonadas, hidratadas e isoméricas [
Otros estudios han realizado el análisis de CA para arándanos usando el equivalente en µmol trolox/g FF muestra a través de CV. Para este estudio la relación fue hallada usando la carga, área bajo la curva del pico de oxidación anódica del extracto del Vaccinium corymbosum. Para este estudio, la muestra que presenta mayor CPT, arroja el mayor CAT y por consiguiente mayor CA mientras que, en el presente trabajo, analizado por la misma técnica, la CA reportada en µmol EAG/g FF, es mayor cuando la muestra tiene mayor CAT, pero menor CPT. Dicha diferencia puede deberse a la técnica de extracción y a los tipos de solvente utilizados. Ambos estudios tienen en común que se correlaciona fuertemente la CA con el CAT [
A modo general, se observó que realizando la extracción por solventes usando etanol puede arrastrar el mayor contenido de polifenoles totales, la mezcla etanol/ácido acético realiza una mayor extracción de antocianinas. Esto puede deberse que a pH ácidos, las antocianinas son protonadas formando un catión [
Si bien las técnicas electroquímicas representan ciertas ventajas con respecto a los demás métodos analíticos para la evaluación de la capacidad antioxidante de los compuestos fenólicos presentes en los arándanos, éstas solo contribuyen a fortalecer la perfilación y/o caracterización de las propiedades bioactivas del fitoquímico dentro del compendio de métodos existentes para tal fin.
En la Figura 7 se evidencia como el valor promedio de la capacidad antioxidante obtenida con el tratamiento EtOH/CH3COOH/H2O difiere significativamente del tratamiento con etanol o con ácido acético, lo que soporta lo discutido anteriormente sobre la importancia de la sinergia entre un solvente prótico en solución acuosa, ligeramente acidulado.
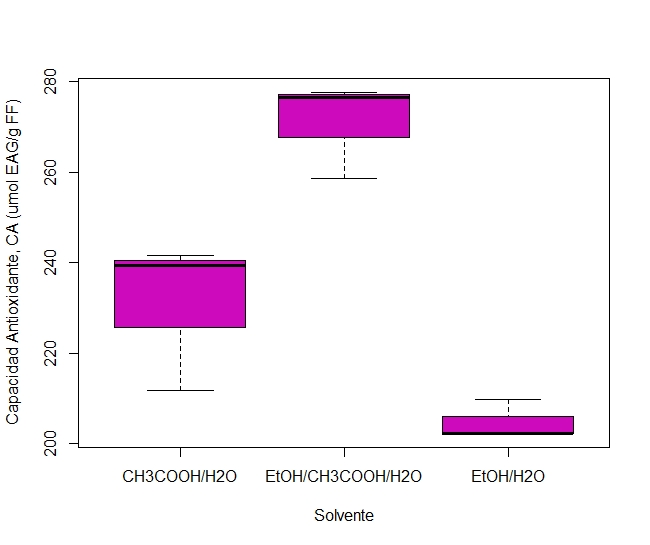
Fuente: elaboración propia.
Para la evaluación estadística de las relaciones entre la capacidad antioxidante con el contenido de polifenoles totales y específicamente con el contenido de antocianinas monoméricas, se evaluaron las correlaciones (Tabla 4).
del CPT vs CA y CAT vs CA. Fuente: elaboración propia.
| Correlaciones | Coeficiente de correlación múltiple, r | Valor de F calculado | Valor crítico de F |
| Contenido de Polifenoles Totales vs Capacidad antioxidante (CPT vs CA) | 0.9991 | 562.319 | 0.027 |
| Contenido de Antocianinas Totales vs Capacidad antioxidante (CAT vs CA) | 0.9653 | 9.921 | 0.195 |
Las correlaciones entre la capacidad antioxidante con el CPT y el CAT, muestran una asociación fuerte que permite identificar como los tratamientos de solventes propuestos se comportan de forma lineal, para ambos indicadores, permitiendo a futuro hacer posibles predicciones, de cómo el comportamiento del contenido de polifenoles con respecto a ambos indicadores, se ve afectada al introducir variables como cambio en las proporciones de los solventes y la presencia o ausencia de acidulantes débiles como el CH3COOH. En adición, el análisis de la regresión lineal o bondad de ajuste permitió evidenciar la dirección de las asociaciones evaluadas, como se muestra en la Figura 8.

De la Figura 8 se puede identificar que la relación de la CA con el CPT es inversa y con CAT, directa, lo cual conlleva a inferir que la presencia de antocianinas está ejerciendo un efecto antioxidante relevante y aunque no expliquen en alta proporción el CPT, si logran tener una relación “fuerte”, lo cual permite evidenciar como el CAT se ve afectada de manera directa en la capacidad antioxidante si se acidifica el sistema de solventes de extracción.
Contrario es el comportamiento con los compuestos fenólicos, los cuales pueden ser una variedad importante, pero que indica que se puede obtener más CPT con ETOH/H2O, pero su capacidad antioxidante se verá menguada de forma significativa estadísticamente.
3.3 Evaluación del riesgo de los solventes
"La selección de solventes verdes son las rutas más eficaces para reducir el impacto medioambiental" [
ambiente. Fuente: Adaptado de [
| Solvente | Puntaje seguridad | Puntaje salud | Puntaje Ambiente | Clasificación |
| Agua* | 1 | 1 | 1 | Recomendado |
| Etanol* | 4 | 3 | 3 | Recomendado |
| Ácido Acético* | 3 | 7 | 3 | Problemático |
| Metano | 4 | 7 | 5 | Problemático |
| Acetona | 5 | 3 | 5 | Problemático |
| Acetonitrilo | 4 | 3 | 3 | Recomendado |
*Solventes utilizados en el estudio.
Evaluación del riesgo: recomendado 1-3; problemático 4-6; y > 7, peligroso.
De acuerdo con la Tabla 5, se evidencia que el empleo de solventes como agua y etanol no representan un riesgo significativo con base a los 3 criterios anteriormente mencionados. Sin embargo, a pesar de que el ácido acético representa un problema de acuerdo con su clasificación cabe resaltar que se empleó a una baja concentración lo que disminuye su riesgo.
Dentro de los demás solventes empleados por los autores, solo el acetonitrilo cumple los criterios propuestos por la CHEM21, lo que hace imperativa la búsqueda de nuevas soluciones verdes y optimización en la obtención de compuestos antioxidantes de los arándanos.
Uno de principales objetivos de la química verde se basa en reducir significativamente el uso y la producción de derivados químicos con una mirada hacia las fuentes renovables. De acuerdo con lo anterior, la gran variedad de disolventes, sobre todo los de carácter orgánico, son dañinos, tóxicos y nocivos en el contexto medioambiental. Por tanto, comprender las propiedades de los disolventes es un factor de relevancia en el desarrollo sostenible [
Dentro de los disolventes que se han sugerido en la literatura como “verdes” se ha reportado el agua, fluidos supercríticos, líquidos iónicos, polímeros líquidos y disolventes derivados de biomasa [
Análogamente, un disolvente se puede considerar verde cuando es más adecuado que el actual para una aplicación concreta. De hecho, no existe ningún disolvente completamente ecológico y, por tanto, siempre dependerá del contexto de su aplicación y de varios requerimientos como restricciones medioambientales (emisiones de compuestos orgánicos volátiles, biodegradabilidad, capa de ozono, y efecto invernadero), eficacia (costo, selectividad, disponibilidad, y poder del solvente) y, finalmente, de seguridad y legislación (riesgo de exposición, toxicidad, inflamabilidad y permiso legal de uso) [
No obstante, dentro de la química de los compuestos bioactivos se ha introducido el concepto de extracción verde de productos naturales que se basa en el desarrollo y diseño de procesos de extracción que reduzcan notablemente el consumo energético y permitan proponer el empleo de disolventes alternativos que garanticen la obtención de extractos seguros y de calidad que parten de la optimización e innovación de los procesos de extracción, el uso de equipos, y el empleo de solventes alternativos en alusión a los 6 principios de la extracción verde de productos naturales [
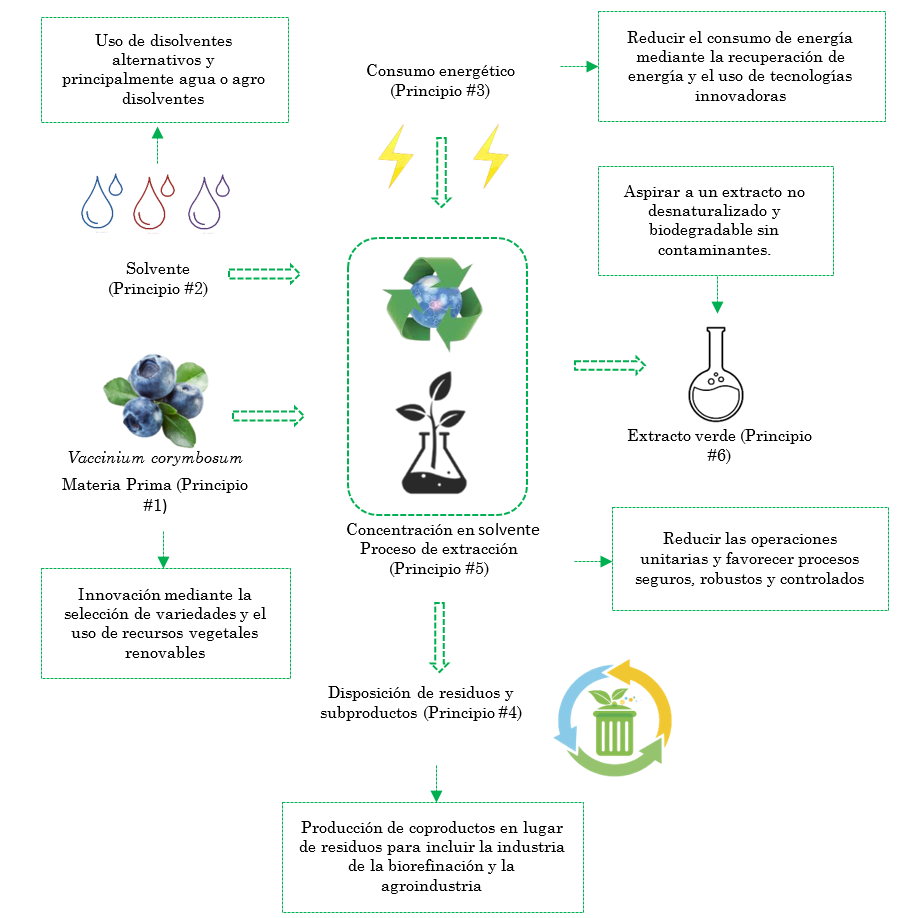
Finalmente, la extracción ecológica de compuestos bioactivos podría ser un paso con un énfasis en la protección del medio ambiente, la seguridad y el desarrollo de la química verde y al mismo tiempo, mejorar la competencia a nivel industrial promoviendo el desarrollo de procesos ecológicos, económicos e innovadores [
4. CONCLUSIONES
Con los tres sistemas de solventes utilizados en este trabajo, se logró la extracción de polifenoles a partir de arándanos Vaccinium corymbosum con resultados comparables con métodos antes reportados, lo cual es una alternativa sostenible al tratarse de solventes verdes amigables con el medioambiente, económicos y con una eficiencia esperada además de ser solventes aprobados por el Codex Alimentarius para su uso.
La evaluación estadística permitió identificar el tipo de correlaciones entre el CAT y CPT con la capacidad antioxidante CA, para identificar el aporte que cada uno de los sistemas de solventes evaluados contribuyeron en la obtención de un extracto a partir un fruto promisorio como materia prima, para tener como referencia en el desarrollo futuro de un ingrediente funcional, orientado al aporte de la capacidad antioxidante, ya sea con un interés por presentar un mayor contenido de polifenoles totales extrayendo con EtOH/H2O, o ser específico en el aporte de antocianinas poliméricas empleando (EtOH/CH3COOH/H2O).
La técnica de CV además de ser económica, sensible, rápida y de fácil empleo, contribuye a fortalecer la caracterización de compuestos bioactivos antioxidantes.
5. AGRADECIMIENTOS
Los autores agradecen a la convocatoria Jóvenes Investigadores e Innovadores ITM 2021 por su financiamiento, y al proyecto P20245 “Evaluación de la capacidad antioxidante y función biológica de un extracto y jugo obtenido a partir de la uva Isabella (Vitis labrusca) mediante la caracterización del perfil quimiométrico y de la actividad citotóxica y antitumoral: una opción para ampliar la aplicación de un ingrediente funcional” de la convocatoria interna ITM–2019.
Los autores Carolina Ramírez y Juan Fernando Bedoya agradecen al semillero de retos químicos (SERQ) del Instituto Tecnológico Metropolitano, ITM.
CONFLICTO DE INTERÉS
Los autores no presentan conflicto de intereses.
CONTRIBUCIÓN DE LOS AUTORES
Juan Fernando Bedoya Cataño contribuyó en la experimentación, análisis bibliográfico, evaluación del diseño experimental, evaluación del riesgo del solvente y redacción del manuscrito.
Carolina Ramón Palacio contribuyó con la experimentación de polifenoles totales y antocianinas.
Maritza Andrea Gil Garzón aportó en el análisis de resultados, el diseño experimental, análisis bibliográfico y redacción del manuscrito.
Carolina Ramírez Sánchez diseño del método electroquímico y aportó en el análisis bibliográfico, redacción y estructuración del manuscrito.
6. REFERENCIAS
- arrow_upward [1] V. Kraujalytė; P. R. Venskutonis; A. Pukalskas; L. Česonienė; R. Daubaras, “Antioxidant properties, phenolic composition and potentiometric sensor array evaluation of commercial and new blueberry (Vaccinium corymbosum) and bog blueberry (Vaccinium uliginosum) genotypes”, Food Chem., vol. 188, pp. 583–590, Dec. 2015. https://doi.org/10.1016/J.FOODCHEM.2015.05.031
- arrow_upward [2] J. Ávila-Román et al., “Phenolic compounds and biological rhythms: Who takes the lead?”, Trends Food Sci. Technol., vol. 113, pp. 77–85, Jul. 2021.https://doi.org/10.1016/j.tifs.2021.04.050
- arrow_upward [3] L. Ge; S.-P. Li; G. Lisak, “Advanced sensing technologies of phenolic compounds for pharmaceutical and biomedical analysis”, J. Pharm. Biomed. Anal., vol. 179, p. 112913, Feb. 2020. https://doi.org/10.1016/j.jpba.2019.112913
- arrow_upward [4] J. Viganó et al., “Comprehensive analysis of phenolic compounds from natural products: Integrating sample preparation and analysis”, Anal. Chim. Acta, vol. 1178, p. 338845, Sep. 2021. https://doi.org/10.1016/j.aca.2021.338845
- arrow_upward [5] C. Ramón; M. A. Gil-Garzón, “Efecto de los parámetros de operación de la extracción asistida por ultrasonido en la obtención de polifenoles de uva: una revisión”, TecnoLógicas, vol. 24, no. 51, p. e1822, Jun. 2021. https://doi.org/10.22430/22565337.1822
- arrow_upward [6] D. Granato; J. S. Santos; L. G. Maciel; D. S. Nunes, “Chemical perspective and criticism on selected analytical methods used to estimate the total content of phenolic compounds in food matrices”, TrAC Trends Anal. Chem., vol. 80, pp. 266–279, Jun. 2016. https://doi.org/10.1016/j.trac.2016.03.010
- arrow_upward [7] A. Chiorcea‐Paquim; T. A. Enache; E. De Souza Gil; A. M. Oliveira‐Brett, “Natural phenolic antioxidants electrochemistry: Towards a new food science methodology”, Compr. Rev. Food Sci. Food Saf., vol. 19, no. 4, pp. 1680–1726, Jul. 2020. https://doi.org/10.1111/1541-4337.12566
- arrow_upward [8] J. Hoyos-Arbeláez; M. Vázquez; J. Contreras-Calderón, “Electrochemical methods as a tool for determining the antioxidant capacity of food and beverages: A review”, Food Chem., vol. 221, pp. 1371–1381, Apr. 2017. https://doi.org/10.1016/j.foodchem.2016.11.017
- arrow_upward [9] A. Aires; R. Carvalho; M. Matos; V. Carnide; A. P. Silva; B. Gonçalves, “Variation of chemical constituents, antioxidant activity, and endogenous plant hormones throughout different ripening stages of highbush blueberry (Vaccinium corymbosum L.) cultivars produced in centre of Portugal”, J. Food Biochem., vol. 41, no. 6, p. e12414, Dec. 2017. https://doi.org/10.1111/jfbc.12414
- arrow_upward [10] G. Ozkan; S. ErcislI; A. Zeb; G. Agar; H. I. Sagbas; G. Ilhan, “Some Morphological and Biochemical Characteristics of Wild Grown Caucasian Whortleberry (Vaccinium arctostaphylos L.) Genotypes from Northeastern Turkey”, Not. Bot. Horti Agrobot. Cluj-Napoca, vol. 47, no. 2, pp. 378–383, Dec. 2018. https://doi.org/10.15835/nbha47111288
- arrow_upward [11] A. Lončarić et al., “Green Extraction Methods for Extraction of Polyphenolic Compounds from Blueberry Pomace”, Foods, vol. 9, no. 11, p. 1521, Oct. 2020. https://doi.org/10.3390/foods9111521
- arrow_upward [12] G.-I. Hidalgo; M. Almajano, “Red Fruits: Extraction of Antioxidants, Phenolic Content, and Radical Scavenging Determination: A Review”, Antioxidants, vol. 6, no. 1, p. 7, Jan. 2017. https://doi.org/10.3390/antiox6010007
- arrow_upward [13] J. Martín-Gómez; M. Á. Varo, J. Mérida; M. P. Serratosa, “Influence of drying processes on anthocyanin profiles, total phenolic compounds and antioxidant activities of blueberry (Vaccinium corymbosum)”, LWT, vol. 120, p. 108931, Feb. 2020. https://doi.org/10.1016/J.LWT.2019.108931
- arrow_upward [14] M. D. Nikolić et al., “Use of cyclic voltammetry to determine the antioxidant capacity of berry fruits: correlation with spectrophotometric assays”, Eur. J. Hortic. Sci., vol. 84, no. 3, pp. 152–160, Jun. 2019. https://doi.org/10.17660/eJHS.2019/84.3.5
- arrow_upward [15] C. Giovagnoli-Vicuña; S. Pizarro; V. Briones-Labarca; Á. Delgadillo, “A Square Wave Voltammetry Study on the Antioxidant Interaction and Effect of Extraction Method for Binary Fruit Mixture Extracts”, J. Chem., vol. 2019, pp. 1–10, Oct. 2019. https://doi.org/10.1155/2019/8706061
- arrow_upward [16] D. Prat et al., “CHEM21 selection guide of classical- and less classical-solvents”, Green Chem., vol. 18, no. 1, pp. 288–296, 2016. https://doi.org/10.1039/c5gc01008j
- arrow_upward [17] L. F. Ferreira et al., “Citric acid water-based solution for blueberry bagasse anthocyanins recovery: Optimization and comparisons with microwave-assisted extraction (MAE)”, LWT, vol. 133, p. 110064, Nov. 2020. https://doi.org/10.1016/J.LWT.2020.110064
- arrow_upward [18] A. Mizuno; G. Yamada; N. Ohtani, “Natural dye-sensitized solar cells containing anthocyanin dyes extracted from frozen blueberry using column chromatography method”, 2018 IEEE 7th World Conference on Photovoltaic Energy Conversion (WCPEC) (A Joint Conference of 45th IEEE PVSC, 28th PVSEC & 34th EU PVSEC), pp. 1129-1131, Jun. 2018. https://ieeexplore.ieee.org/document/8547843
- arrow_upward [19] C. J. Clarke; W.-C. Tu; O. Levers; A. Bröhl; J. P. Hallett, “Green and Sustainable Solvents in Chemical Processes”, Chem. Rev., vol. 118, no. 2, pp. 747–800, Jan. 2018. https://doi.org/10.1021/acs.chemrev.7b00571
- arrow_upward [20] T. Welton, “Solvents and sustainable chemistry”, Proc. R. Soc. A Math. Phys. Eng. Sci., vol. 471, no. 2183, p. 20150502, Nov. 2015. https://doi.org/10.1098/rspa.2015.0502
- arrow_upward [21] K. Häckl; W. Kunz, “Some aspects of green solvents” Comptes Rendus Chim., vol. 21, no. 6, pp. 572–580, Jun. 2018. https://doi.org/10.1016/j.crci.2018.03.010
- arrow_upward [22] F. Chemat et al., “Green extraction of natural products. Origins, current status, and future challenges,” TrAC - Trends Anal. Chem., vol. 118, pp. 248–263, Sep. 2019. https://doi.org/10.1016/j.trac.2019.05.037
- arrow_upward [23] Z. Idham; I. I. Muhamad; M. R. Sarmidi, “Degradation kinetics and color stability of spray-dried encapsulated anthocyanins from Hibiscus sabdariffa L.”, J. Food Process Eng., vol. 35, no. 4, pp. 522–542, Aug. 2012. https://doi.org/10.1111/j.1745-4530.2010.00605.x
- arrow_upward [24] A. Bunea; O. D. Rugina; A. M. Pintea; Z.Sconţa; C. I. Bunea; C. Socaciu, “Comparative Polyphenolic Content and Antioxidant Activities of Some Wild and Cultivated Blueberries from Romania”, Not. Bot. Horti Agrobot. Cluj-Napoca, vol. 39, no. 2, pp. 70-76, Nov. 2011. https://doi.org/10.15835/nbha3926265
- arrow_upward [25] W. E. Espinoza Manrique; L. C. A. Garzón Salcedo; O. J. Medina Vargas, “Validación de una metodología analítica para la cuantificación de polifenoles totales, en procesos de extracción asistida por microondas sobre frutos de la especie colombiana Vaccinium meridionale”, Rev. Colomb. Ciencias Químico Farm., vol. 45, no. 1, pp. 109–126, 2016. http://www.scielo.org.co/scielo.php?pid=S0034-74182016000100007&script=sci_abstract&tlng=es
- arrow_upward [26] N. Benbouguerra; T. Richard; C. Saucier; F. Garcia, “Voltammetric behavior, flavanol and anthocyanin contents, and antioxidant capacity of grape skins and seeds during ripening (Vitis vinifera var. merlot, Tannat, and Syrah)”, Antioxidants, vol. 9, no. 9, pp. 1–19, Aug. 2020. https://doi.org/10.3390/antiox9090800
- arrow_upward [27] M. J. Rebelo; R. Rego; M. Ferreira; M. C. Oliveira, “Comparative study of the antioxidant capacity and polyphenol content of Douro wines by chemical and electrochemical methods”, Food Chem., vol. 141, no. 1, pp. 566–573, Nov. 2013. https://doi.org/10.1016/j.foodchem.2013.02.120
- arrow_upward [28] C. Aristizábal; A. F. Vargas; P. N. Alvarado, “Numerical determination of the correct solvents to extract a phytochemical from coffee pulp using Hansen solubility parameters, risk assessment, sustainability evaluation, and economic analysis”, DYNA, vol. 86, no. 211, pp. 138–147, Oct. 2019. https://doi.org/10.15446/dyna.v86n211.78530
- arrow_upward [29] F. Chemat; M. A. Vian; G. Cravotto, “Green extraction of natural products: Concept and principles”, Int. J. Mol. Sci., vol. 13, no. 7, pp. 8615–8627, Jul. 2012. https://doi.org/10.3390/ijms13078615
- arrow_upward [30] S. C. Moldoveanu; V. David, “Mobile Phases and Their Properties”, in Essentials in Modern HPLC Separations, Elsevier, 2013, pp. 363–447. https://doi.org/10.1016/b978-0-12-385013-3.00007-0
- arrow_upward [31] S. Wahyuningsih; L. Wulandari; H. Munawaroh; A. H. Ramelan, “The Effect of pH and Color Stability of Anthocyanin on Food Colorant”, Int. Conf. Food Sci. Eng., vol. 193, 2017. https://doi.org/10.1088/1757-899X/193/1/012047
- arrow_upward [32] E. Rodrigues; N. Poerner; I. I. Rockenbach; L. V. Gonzaga; C. R. Mendes; R. Fett, “Phenolic compounds and antioxidant activity of blueberry cultivars grown in Brazil”, Food Sci. Technol., vol. 31, no. 4, pp. 911–917, Dec. 2011. https://doi.org/10.1590/s0101-20612011000400013
- arrow_upward [33] G. Giovanelli; S. Buratti, “Comparison of polyphenolic composition and antioxidant activity of wild Italian blueberries and some cultivated varieties”, Food Chem., vol. 112, no. 4, pp. 903–908, Feb. 2009. https://doi.org/10.1016/j.foodchem.2008.06.066
- arrow_upward [34] G. L. Fabiani; E. E. Pérez; L. Corral; A. R. Salguero; M. González; M. L. Tereschuk; H. J. Boggetti, “Evaluación del contenido de antioxidantes en extractos convencionales y supercríticos de arándano (Vaccinium corymbosum L.)”, Investig. en Fac. Ing. del NOA., pp. 1-6, Oct. 2013. https://blueberriesconsulting.com/evaluacion-del-contenido-de-antioxidantes-en-extractos-convencionales-y-supercriticos-de-arandano-vaccinium-corymbosum-l/
- arrow_upward [35] Consejo Superior de Política Fiscal, “Resolución número 0001 de 2015, por la cual se modifica el presupuesto de una Empresa Industrial y Comercial del Estado para la vigencia fiscal de 2015, (30 de diciembre de 2015). Resolución número 0001 de 2015, por la cual se modifica el presupuesto de una Empresa Industrial y Comercial del Estado para la vigencia fiscal de 2015 - 13 de Febrero de 2015 - Diario Oficial de Colombia - Legislación - VLEX 557502562
- arrow_upward [36] N. Colak et al., “Comparison of Phenolics and Phenolic Acid Profiles in Conjunction with Oxygen Radical Absorbing Capacity (ORAC) in Berries of Vaccinium arctostaphylos L. and V. myrtillus L.”, Polish J. Food Nutr. Sci., vol. 66, no. 2, pp. 85–91, 2016. https://doi.org/10.1515/pjfns-2015-0053
- arrow_upward [37] V. Dragović-Uzelac; Z. Savić; A. Brala; B. Levaj; D. Bursać Kovaćević; A. Biško, “Evaluation of phenolic content and antioxidant capacity of blueberry cultivars (Vaccinium corymbosum L.) grown in the northwest Croatia”, Food Technol. Biotechnol., vol. 48, no. 2, pp. 214–221, 2010. https://repozitorij.pbf.unizg.hr/islandora/object/pbf:3092
- arrow_upward [38] A. M. Mustafa et al., “A new HPLC-MS/MS method for the simultaneous determination of 36 polyphenols in blueberry, strawberry and their commercial products and determination of antioxidant activity”, Food Chem., vol. 367, p. 130743, Jan. 2022. https://doi.org/10.1016/j.foodchem.2021.130743
- arrow_upward [39] M. Shi; H. Loftus; A. J. McAinch; X. Q. Su, “Blueberry as a source of bioactive compounds for the treatment of obesity, type 2 diabetes and chronic inflammation”, J. Funct. Foods, vol. 30, pp. 16–29, Mar. 2017. https://doi.org/10.1016/j.jff.2016.12.036
- arrow_upward [40] J. Muselík; M. García-Alonso; M. P. Martín-López; M. Žemlička; J. C. Rivas-Gonzalo, “Measurement of antioxidant activity of wine catechins, procyanidins, anthocyanins and pyranoanthocyanins”, Int. J. Mol. Sci., vol. 8, no. 8, pp. 797–809, Aug. 2007. https://doi.org/10.3390/i8080797
- arrow_upward [41] J. Koh; Z. Xu; L. Wicker, “Binding kinetics of blueberry pectin-anthocyanins and stabilization by non-covalent interactions”, Food Hydrocoll., vol. 99, p. 105354, Feb. 2020. https://doi.org/10.1016/j.foodhyd.2019.105354
 PDF
PDF
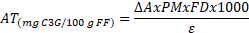 (1)
(1)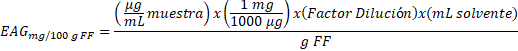 (2)
(2)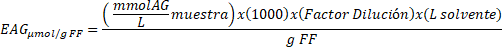 (3)
(3)