Potencial agroindustrial del epicarpio de mandarina como alternativa de colorante natural en pan
Agro-Industrial Potential of the Mandarina Epicarp a Natural Coloring Allternative in Bread
Recibido: 10 de agosto de 2019
Aceptado: 12 de diciembre de 2019
Resumen
En este estudio se evaluó el potencial agroindustrial de la harina de epicarpio de mandarina Oneco (Citrus reticulata) como posible colorante natural en el pan. En la metodología se analizaron las propiedades fisicoquímicas como el pH, aw, los parámetros de color: luminosidad (L*), cromaticidad (C*) y ángulo de tono (h°), porcentaje de acidez, porcentaje de materia seca, cuantificación de carotenoides por espectrofotometría, compuestos fenólicos, capacidad antioxidante en harina y parámetros de color (L*, C* y h°) en el pan. Se encontró que, después del tratamiento de secado convectivo, se retuvieron concentraciones significativamente más altas de compuestos bioactivos como los fenólicos, se evidenció también un aumento en la capacidad antioxidante y el contenido de carotenoides, además de cambios significativos en los parámetros de color (L* y C*). En la sustitución de la harina de epicarpio de mandarina en las formulaciones del pan, se notó un aumento significativo en la concentración del contenido de carotenoides, siendo el pico de esta en la sustitución del 4 %; En los parámetros de color, se hallaron diferencias significativas en los parámetros L* y C*, presentando el mayor valor de L* en la sustitución del 2 % y de C* en la sustitución del 4 %, mientras que el parámetro h° no presentó diferencias significativas en ninguna de las formulaciones. Finalmente, se concluye que la harina de epicarpio de mandarina puede ser una alternativa importante, como aditivo de colorante natural en la elaboración del pan.
Palabras clave: Carotenoides, compuestos fenólicos, capacidad antioxidante, cítrico, cromaticidad
Abstract
This study evaluated the agro-industrial potential of flour made of the epicarp of Oneco mandarin (Citrus reticulata) as a possible natural bread coloring. We analyzed the physiochemical properties of said fruit, such as pH, aw, color parameters (luminosity, L*; chromaticity, C*; and pitch angle, h°), acidity percentage, dry matter percentage, quantification of carotenoids by spectrophotometry, phenolic compounds, antioxidant capacity in flour, and color parameters (L*, C*, and h°) in bread. We found that, after convective drying, the fruit retained significantly higher concentrations of bioactive compounds, such as phenols. We also observed an increase in antioxidant capacity and carotenoid content, in addition to significant changes in the color parameters (L* and C*). When the mandarin epicarp flour substituted conventional flour in the bread formula, we noted a significant increase in the concentration of the carotenoid content; the peak of this substitution was 4%. Regarding color, parameters L* and C* exhibited significant differences; L* was higher in the 2% substitution, while C* was higher in the 4% substitution, and h° did not present significant differences in any of the formulas. Finally, we conclude that mandarin epicarp flour can be an important alternative additive for natural coloring in bread making.
Keywords: Carotenoids, Phenolic compounds, Antioxidant capacity, Citric, Chromaticity
1. INTRODUCCIÓN
Los cítricos son uno de los cultivos frutales más importantes del mundo, con una producción anual de aproximadamente 102 millones de toneladas [
El procesamiento de los cítricos genera subproductos que pueden alcanzar hasta el 50 % del peso original de la fruta, siendo el epicarpio el subproducto principal [
Estos subproductos son fuentes importantes de aceite esencial, carotenoides y compuestos fenólicos, que los convierte en recursos atractivos en la valoración agroindustrial como fuente importante de aditivos en la industria alimentaria, cosmética y farmacéutica [
Se han realizado varios estudios sobre la caracterización de frutas cítricas, como los llevados a cabo por [
Se han adelantado varios estudios sobre el uso de harinas de epicarpio y mesocarpio de frutas en productos horneados. [
En la actualidad son limitados los estudios en la valoración de los subproductos generados en el procesamiento de críticos en Colombia que permitan identificar el potencial agroindustrial del epicarpio de mandarina como fuente de aditivos naturales en la industria alimentaria, cosmética y farmacéutica. En razón a esto, el objetivo de la presente investigación fue evaluar el potencial agroindustrial de la harina de epicarpio de mandarina Oneco (Citrus reticulata) como posible colorante natural en el pan.
2. MATERIALES Y MÉTODOS
2.1 Acondicionamiento de material primo
De un supermercado ubicado en la galería Alameda en la ciudad de Santiago de Cali (Valle del Cauca), se adquirieron 20 kg de mandarina Oneco (Citrus reticulata) en estado de madurez de consumo, de los cuales se obtuvieron 4kg de epicarpio aproximadamente. La mandarina fue lavada en una solución jabonosa 1:4, desinfectada con hipoclorito a 100ppm durante 5 min y pelada manualmente. El epicarpio (cáscara) de la mandarina fue troceado en julianas de 2,8 mm de espesor y 6,5 cm de longitud aproximadamente, sumergido en una solución de metasulfito a 100ppm durante 5 min, escaldado durante 2 min a 85 ºC y congelado con el fin de reducir el tiempo de secado. El epicarpio fue tratado durante 4 horas aproximadamente en un secador de bandejas convectivo a 40 ºC y velocidad de flujo a 3m/s, hasta obtener una humedad constante de 8 %. Se redujo el tamaño del epicarpio deshidratado en un molino de cuchillas IKA Labortchnik M hasta que el 98 % de la harina pasó por una malla US 200. Posteriormente, la harina de epicarpio de mandarina fue almacenada en un frasco de vidrio bajo refrigeración a una temperatura de 4 ºC [
2.2 Aplicación de la harina de epicarpio de mandarina en el pan
El pan se elaboró siguiendo la metodología de [
Se realizaron cuatro tratamientos, el primer tratamiento fue el control con 0,03 g de tartrazina y los otros tres tratamientos fueron sustituciones de harina de trigo por harina de epicarpio de mandarina a 2 %, 3 % y 4 %.
2.3 Determinaciones fisicoquímicas
A las muestras de estudio se le hicieron mediciones de materia seca siguiendo el protocolo [
2.4 Determinación del color superficial CIEL*a*b*
Se les determinó el color a las muestras de estudio mediante la lectura de las coordenadas L*, a* y b* en un colorímetro Konica Minolta CR-400. El colorímetro se estandarizó con una baldosa negra y una blanca (Y= 89,5; x= 0,3176; y y= 0,3347) usando el iluminante D65 y un observador 2º. Los valores numéricos de L*, a* y b* se convirtieron en croma (C*), y ángulo de matiz (hº) según [
C*=(a*2+b*2)1/2 (1)
h-º=tan-1(b*/a*) (2)
2.5 Determinación del contenido de carotenoides
Los carotenoides se cuantificaron siguiendo la metodología de [
Posteriormente, se sometieron a agitación a 140 rpm en una plancha de agitación durante 1 h. Transcurrido el tiempo se adicionó 1 ml de agua destilada y se sometieron a agitación durante 10 min más.
Se visualizó una separación de fases; en la parte superior el hexano y en la parte inferior el etanol y agua. Se leyó en el espectrofotómetro Spectrophotometer Jenway 6320D, USA la fase orgánica (hexano) a 450, 444, 451 y 472 nm para β-caroteno, α-caroteno, β-criptoxantina, zeaxantina y licopeno respectivamente. El contenido de carotenoides disueltos en hexano se calculó mediante (3):
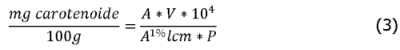
2.6 Determinación de compuestos fenólicos totales
La concentración de fenoles totales se determinó siguiendo la metodología de [
Pasado este tiempo se filtró el extracto y se tomaron y mezclaron 0,5 ml del extracto con 5 ml de agua destilada y 0,5 ml de reactivo de Folin-Ciocalteu; entonces, se dejó que la mezcla reaccionara durante 2 min a temperatura ambiente.
Pasado el tiempo, se adicionó 1 ml de carbonato de sodio anhídrido al 20 % y se sometieron los tubos a baño térmico durante 15 min a 45 ºC. Se dejó enfriar a temperatura ambiente las muestras. La absorbancia de las muestras se midió a 765 nm usando el espectrofotómetro Spectrophotometer Jenway 6320D, USA.
Para la determinación de fenoles totales, se hizo una curva de calibración (0,002 a 0,017 mg de ácido gálico (AG) por ml de solución, con una correlación de 99,55 %). Los valores fueron expresados en mg de ácido gálico /100 g de muestra b.s
2.7 Determinación de la capacidad antioxidante (% dpph)
La capacidad antioxidante expresada como porcentaje de inhibición del radical dpph 2,2-diphenyl-1-picrylhydrazyl, se determina siguiendo la metodología de [
Pasado este tiempo, se filtró el extracto y se tomó 1 ml de este para mezclarlo con 2 ml del reactivo dpph 0,1 mM recién preparado. Se elaboró un control con 1 ml de metanol y 2 ml de dpph recién preparado. Se dejaron en reposo durante 1 h en la oscuridad la muestra y el control.
Luego se midió la absorbancia de la muestra y el control usando el espectrofotómetro Spectrophotometer Jenway 6320D, USA a una longitud de onda de 517 nm.
El porcentaje de actividad antioxidante en términos de inhibición del radical dpph se determinó mediante (4):

2.8 Análisis estadístico
La comparación de medias de los tratamientos fresco y deshidratado y la diferencia entre ellos se determinó mediante una prueba T-Student, y el efecto de la inclusión del epicarpio de mandarina en el pan se estableció por medio de un diseño experimental aleatorizado simple con cuatro tratamientos (control, 2 %, 3 % y 4 %) y una prueba Tukey para observar las diferencias entre los tratamientos. El tratamiento de datos es evaluado en el paquete estadístico minitab V17 con un nivel de confianza del 95 %. La experimentación de todos los tratamientos se hizo por triplicado y se llevó a cabo en el laboratorio de Frutas y Hortalizas de la Universidad Nacional de Colombia sede Palmira.
3. RESULTADOS Y DISCUSIÓN
En la Tabla 1 se presentan los valores medios evaluados de los parámetros fisicoquímicos: color superficial CIEL*a*b*, fenoles totales y capacidad antioxidante (% dpph), evaluada en el epicarpio de mandarina en fresco y deshidratado. El análisis estadístico evidencia un efecto significativo en las variables de estudio después del proceso de deshidratación, excepto en la variable de color h°.
Los valores de porcentaje materia seca (% materia seca), aw, pH, L*, y C* del material en fresco superan significativamente los valores obtenidos en el material deshidratado, por el contrario, la acidez (% acidez), los fenoles totales y la actividad antioxidante son significativamente mayores en el material deshidratado (Tabla 1).
Tabla 1. Parámetros fisicoquímicos del epicarpio de mandarina en fresco y deshidratado
Fuente: elaboración propia.
| Muestra 1 | Fresco | Deshidratado | T-Studet |
| % Materia Seca | 16,16±1,58 | 91,63±2,52 | *** |
| aw | 0,995±0,00 | 0,42±0,06 | *** |
| pH | 5,19±0,10 | 4,82±0,01 | ** |
| % acidez2 | 11,52±1,28 | 15,79±2,41 | * |
| Fenoles totales 3 | 19,81±0,60 | 27,07±2,68 | ** |
| % dpph | 53,27±2,80 | 88,79±0,93 | *** |
| L* | 49,97±0,68 | 39,74±0,05 | *** |
| C* | 43,82±1,26 | 25,08±0,13 | *** |
| hº degree | 81,99±4,55 | 86,38±0,05 | NS |
1 Valores promedios ±DS (n=3)
2 Valores expresados en equivalentes de ácido cítrico/ 100g b.s
3 Valores expresados en mg de ácido gálico /100g de muestra b.s
(*): significativo p<0,05; (**): significativo p<0,01; (***): significativo p<0,001; para dos muestras
NS: no hay diferencias significativas
El epicarpio de mandarina es deshidratado hasta alcanzar un porcentaje de materia seca de 91,63±2,52 % y una actividad de agua de 0,42±0,06. El decrecimiento del agua disponible permite prolongar la vida útil de la misma, disminuyendo la proliferación de bacterias, hongos, mohos y reacciones enzimáticas de deterioro.
El epicarpio de mandarina en fresco presenta un pH de 5,19±0,10 y un porcentaje de acidez de 11,52±1,28, mientras que el epicarpio de mandarina deshidratada registró un pH de 4,82±0,01 y un porcentaje de acidez de 15,79±2,41.
Estos cambios en las muestras evaluadas después del tratamiento térmico pueden estar asociados a los procesos de lixiviación y oxidación de los compuestos orgánicos cuando la matriz biológica es afectada por la temperatura [
El epicarpio de mandarina presenta bajos niveles de compuestos fenólicos totales; 19,81±0,60 y 27,07±2,68 mg de ácido gálico/100 g de muestra, en fresco y deshidratado respectivamente. De acuerdo con la clasificación propuesta por [
Esto concuerda con los resultados obtenidos por [
Los compuestos fenólicos son sustancias que poseen un anillo aromático y un anillo de benceno con uno o más grupos de hidróxido, que incluyen derivados funcionales (como ésteres, ésteres metílicos, glucósidos, etc.) [
El 1,1-difenil-2-picrilhidrazilo (radical dpph) es un radical libre estable centrado en nitrógeno, al aceptar un radical de hidrógeno o un electrón, el dpph se convierte en una molécula diamagnética estable que desempeña el papel de un antioxidante [
La capacidad antioxidante de los extractos está influenciada por su composición química y actúa como agente protector reduciendo el daño oxidativo causado en el cuerpo, inhibiendo la peroxidación de los lípidos y retardando el progreso de muchas enfermedades [
Según [1], la capacidad antioxidante de los cítricos está asociada a compuestos como las vitaminas; entre estos se encuentran la vitamina A, que puede reaccionar con los radicales libres, especialmente con el oxígeno singlete (1O2) y los radicales peroxilo; la vitamina C, que puede eliminar eficazmente una variedad de especies reactivas de oxígeno (ros) y desprender ácido semideshidroascórbico, eliminando 1O2 y reduciendo los radicales de azufre; la vitamina E, que puede proteger las membranas celulares contra el daño por la peroxidación de lípidos; minerales como el Mn, Fe, Cu, Zn y Se; compuestos fenólicos como los flavonoides, que pueden eliminar especies reactivas de oxígeno y disminuir la formación de peróxido in vivo; ácidos fenólicos, a través de la deshidrogenación de los grupos hidroxilo; el efecto de la ortosustitución en un anillo de benceno y las curcuminas debido a sus grupos hidroxilo-fenólicos; y compuestos terpenoides como los limonoides, la pectina a través de la mejora de las enzimas antioxidantes endógenas y la eliminación de radicales libres y los carotenoides debido a la eliminación de radicales libres y 1O2.
La reducción de los valores de color superficial L* y C* en las muestras deshidratadas concuerdan con los resultados obtenidos por [
La reducción de estos parámetros de color durante el proceso de deshidratación pueden ser consecuencia de la isomeración de los carotenoides, polimerización y degradación de flavonoides o de las reacciones de pardeamiento no enzimático, tales como condensación de hexosas y componentes de aminoácidos, y la oxidación del ácido ascórbico, tal como lo expresó previamente [
3.2 Concentración de carotenoides en la harina de epicarpio de mandarina
Los carotenoides son tetraterenoides responsables principalmente del color rojo, naranja o amarillo de las frutas y son importantes precursores de la vitamina A [
En la Tabla 2 se presentan los valores de la concentración del contenido de carotenoides evaluados en el epicarpio de la mandarina en fresco y deshidratado. El análisis estadístico revela una diferencia significativa entre las muestras evaluadas.
Fuente: elaboración propia.
| Muestra 1 | Fresco | Deshidratado | T-Student | |
| β- caroteno | 20,81±3,58 | 116,52±0,45 | *** | |
| α- caroteno | 22,16±4,59 | 112,15±3,99 | *** | |
| β-criptoxantina | 21,17±3,24 | 119,06±0,11 | *** | |
| zeaxantina | 21,00±3,21 | 118,10±0,11 | *** | |
| licopeno | 16,58±0,62 | 67,76±2,74 | *** | |
1 Valores promedios ±DS (n= 3); los valores son expresados en mg/100 g de muestra seca
(***): significativo p<0,001, para dos muestras
La retención del contenido de carotenoides obtenidos del epicarpio de mandarina en la muestra deshidratada fue significativamente mayor al material en fresco. Este aumento en la concentración de carotenoides se le atribuye al tratamiento térmico al que fue sometido el material en fresco durante el proceso de deshidratación [
Tratamientos térmicos como el escaldado están asociados con la inhibición de la enzima lipoxigenasa (lox), la cual está relacionada con la destrucción o blanqueado de pigmentos carotenoides [
Se obtiene una concentración significativamente mayor de los carotenoides α- caroteno y β-criptoxantina en el material en fresco, mientras que en el material deshidratado se obtienen concentraciones mayores en los carotenoides β-criptoxantina y zeaxantina.
El carotenoide β-criptoxantina es el responsable de la coloración naranja del epicarpio de mandarina [
El licopeno fue el pigmento que presentó menor concentración tanto en fresco como deshidratado, se presentan concentraciones de 16,58±0,62 mg/100 g de muestra seca y 67,76±2,74 mg/100 g de muestra seca respectivamente.
Este carotenoide es considerado el pigmento con mayor capacidad para eliminar el oxígeno singlete. Los estudios han demostrado que el licopeno protege las moléculas lipídicas, las lipoproteínas de baja densidad, las proteínas y el adn contra los ataques de radicales libres, desempeñando un papel esencial en la protección contra enfermedades [
La concentración obtenida del epicarpio de mandarina deshidratada de β- caroteno y licopeno fue muy elevada comparada con los reportados por [
La concentración obtenida β-criptoxantina en el epicarpio de mandarina fresca fue mayor que la reportada por [
El autor reporta valores de 13,4µg/g en mandarina clementina, 11,4 µg/g en naranja china, 11,3 µg/g en pomelo y 19,9µg/g en limón. Las variaciones de la concentración de carotenoides pueden atribuirse a: las prácticas agrícolas, exposición al sol, el área de producción, la etapa de maduración, el manejo pos cosecha y la metodología utilizada para el análisis [
3.3 Valoración de la harina de epicarpio de mandarina como colorante natural en el pan
Las propiedades fisicoquímicas del pan formulado con las diferentes concentraciones de harina de epicarpio de mandarina se representan en la Tabla 3.
Tabla 3. Concentración de carotenoides y color superficial con diferentes concentraciones de epicarpio de mandarina.
Fuente: elaboración propia.
| Formulaciones | Anova | ||||
| Variables1 | Control | 2 % | 3 % | 4 % | |
| β- caroteno2 | 2,23±1,51d | 5,84±1,95c | 8,96±1,22b | 10,46±1,56a | *** |
| α- caroteno2 | 1,64±1,52d | 4,77±1,91c | 8,19±1,12b | 14,10±1,98a | *** |
| β-criptoxantina2 | 1,28±1,53c | 5,65±1,98b | 6,91±1,63b | 11,30±1,96a | *** |
| Zeaxantina2 | 1,26±1,54c | 4,58±2,64b | 4,78±2,02b | 10,27±2,04a | *** |
| Licopeno2 | 0,88±1,55c | 3,21±1,85b | 3,35±1,42b | 7,20±1,43a | *** |
| L* | 37,19±2,71b | 74,06±1,98a | 73,17±2,04a | 73,25±2,18a | *** |
| C* | 20,42±1,55b | 32,21±0,81a | 35,36±1,44a | 38,51±1,55a | ** |
| hº | 92,95±1,09a | 93,16±0,82a | 92,71±0,53a | 92,44±0,56a | NS |
1Valores promedios ±DS (n=3); Las diferentes letras en cada fila indican una diferencia significativa
(**) p<0,01, (***) p<0,001 entre cada formulación
2 los valores son expresados en mg/100g de muestra seca
El análisis de Anova revela que existen diferencias significativas entre el control y las formulaciones con el subproducto de la mandarina, excepto en el parámetro de color hº (Tabla 3). En el caso de los carotenoides, se observa un aumento significativo de estos pigmentos en el pan al incrementar la harina de epicarpio de mandarina (Tabla 3). [
Por otra parte, al comparar las concentraciones presentes de estos pigmentos en el epicarpio deshidratado y el pan, se observa una reducción de carotenoides (Tabla 2, y 3). Autores como [
En el pan, los atributos de color (L*) y cromaticidad (C*) aumentan significativamente al incrementar el epicarpio de mandarina en la formulación (Tabla 3). Los resultados de L* y C* no se ajustan a los registrados previamente por [
La explicación de esta propiedad en el pan elaborado con epicarpio de mandarina está asociada a la presencia de carotenoides en este subproducto, tal como se ha registrado previamente en la Tabla 2.
4. CONCLUSIONES
En el presente estudio se puede concluir que el epicarpio deshidratado de mandarina de variedad Oneco es una importante fuente de carotenoides y compuestos antioxidantes que podrían ser utilizados como aditivos naturales en la industria alimentaria, farmacéutica y cosmética. Por otra parte, el proceso de deshidratación reduce significativamente la intensidad del color amarillo en el epicarpio de mandarina; sin embargo, este subproducto podría ser una importante alternativa de aditivo colorante natural en la elaboración de pan.
Se recomienda desarrollar estudios sobre estabilidad, calidad y análisis sensorial del pan formulado con la harina de epicapio de mandarina durante el almacenamiento.
5. AGRADECIMIENTOS
Los autores manifiestan su agradecimiento a la Universidad Nacional de Colombia, Sede Palmira, a través del Proyecto Hermes 42088 y al grupo de investigación Procesos Agroindustriales (gipa).
6. REFERENCIAS
- arrow_upward [1] Z. Zou, W. Xi, Y. Hu, C. Nie y Z. Zhou, “Antioxidant activity of Citrus fruits”, Food Chem., vol. 196, pp. 885-896, Abr. 2016. https://doi.org/10.1016/j.foodchem.2015.09.072
- arrow_upward [2] M. F. Martínez, “Caracterización molecular de genotipos de mandarinas citrus spp. mediante marcadores ram´s (microsatélites amplificados al azar) y microsatélites” (tesis de Marestría) Universidad Nacional de Colombia, Palmira, 2013. Disponible en: http://www.bdigital.unal.edu.co/12773/1/7609502.2013.pdf
- arrow_upward [3] Taxonomy Browser, “Trópicos”, 2018. Disponible en: http://legacy.tropicos.org/TaxonomyBrowser.aspx?nameid=28100572&projectid=0&conceptid=1
- arrow_upward [4] H. R. de Moraes Barro, T. A. Pinto de Castro Ferreira y M. I. Genovese, “Antioxidant capacity and mineral content of pulp and peel from commercial cultivars of citrus from Brazil”, Food Chem., vol. 134, no. 4, pp. 1892-1898, 2012. https://doi.org/10.1016/j.foodchem.2012.03.090
- arrow_upward [5] J. Contreras-Calderón, L. Calderón-Jaimes, E. Guerra-Hernández y B. García-Villanova, “Antioxidant capacity, phenolic content and vitamin C in pulp, peel and seed from 24 exotic fruits from Colombia”, Food Res. Int., vol. 44, no.7, pp. 2047-2053, ago. 2011. https://doi.org/10.1016/j.foodres.2010.11.003
- arrow_upward [6] N. M’hiri, I. Ioannou, M. Ghoul y N. Mihoubi Boudhrioua, “Phytochemical characteristics of citrus peel and effect of conventional and nonconventional processing on phenolic compounds: A review”, Food Rev. Int., vol. 33, no.6, pp. 587-619, Jun. 2017. https://doi.org/10.1080/87559129.2016.1196489
- arrow_upward [7] M. Sanz-Puig, P. Moreno, M. C. Pina-Pérez, D. Rodrigo y A. Martínez, “Combined effect of High Hydrostatic Pressure (hhp) and antimicrobial from agro-industrial by-products against S. Typhimurium”, LWT, vol. 77, pp. 126-133, abr. 2017. https://doi.org/10.1016/j.lwt.2016.11.031
- arrow_upward [8] S. Rafiq, R. Kaul, S. A. Sofi, N. Bashir, F. Nazir y G. Ahmad Nayik, “Citrus peel as a source of functional ingredient: A review”, J. Saudi Soc. Agric. Sci., vol. 17, no.4, pp. 351-358, oct. 2018. https://doi.org/10.1016/j.jssas.2016.07.006
- arrow_upward [9] L. M. R. da Silva et al., “Quantification of bioactive compounds in pulps and by-products of tropical fruits from Brazil”, Food Chem., vol. 143, pp. 398-404, ene. 2014. https://doi.org/10.1016/j.foodchem.2013.08.001
- arrow_upward [10] K. M. Yoo y B. K. Moon, “Comparative carotenoid compositions during maturation and their antioxidative capacities of three citrus varieties”, Food Chem., vol. 196, pp. 544-549, abr. 2016. https://doi.org/10.1016/j.foodchem.2015.09.079
- arrow_upward [11] B. B. Mathew, D. Shajie, N. Wadhwa, N. B. Krishna Murthy, T. P. Krishna Murthy y M. Rashmi, “Comparative antioxidant efficacy of Citrus limonum pulp and peel. An in vitro study”, Drug Invent. Today, vol. 5, no.4, pp. 296-301, dic. 2013. https://doi.org/10.1016/j.dit.2013.07.003
- arrow_upward [12] V. Goulas y G. A. Manganaris, “Exploring the phytochemical content and the antioxidant potential of Citrus fruits grown in Cyprus”, Food Chem., vol. 131, no.1, pp. 39-47, Mar. 2012. https://doi.org/10.1016/j.foodchem.2011.08.007
- arrow_upward [13] L. E. Ordóñez-Santos, J. Martínez-Girón y A. M. Figueroa-Molano, “Effect of the addition of peach palm (Bactris gasipaes) peel flour on the color and sensory properties of cakes”, Food Science and Technology, vol. 37 , no.3, pp. 418-424, Jul. 2017. https://doi.org/10.19084/rca16008
- arrow_upward [14] G. D. Singh, C. S. Riar, C. Saini, A. S. Bawa, D. S. Sogi y D. C. Saxena, “Indian water chestnut flour- method optimization for preparation, its physicochemical, morphological, pasting properties and its potential in cookies preparation”, LWT-Food Sci. Technol., vol. 44, no.3, pp. 665-672, abr. 2011. https://doi.org/10.1016/j.lwt.2010.09.015
- arrow_upward [15] L. C. R. dos Reis, E. M. P. Facco, M. Salvador, S. H. Flôres y A. de O. Rios, “Characterization of Orange Passion Fruit Peel Flour and Its Use as an Ingredient in Bakery Products”, J. Culin. Sci. Technol., pp. 1-17. dic. 2018. https://doi.org/10.1080/15428052.2018.1564103
- arrow_upward [16] H. S. Ali, A. Farouk Mansour, M. M. Kamil y A. M. S. Hussein, “Formulation of Nutraceutical Biscuits Based on Dried Spent Coffee Grounds”, Int. J. Pharmacol., vol. 14, no. 4, pp. 584-594, Abr. 2018. https://doi.org/10.3923/ijp.2018.584.594
- arrow_upward [17] D. Potosi Calvache, P. Vanegas Mahecha y H. A. Martínez, Correa, “Convective drying of squash (Cucurbita moschata): Influence of temperature and air velocity on effective moisture diffusivity, carotenoid content and total phenols”, Dyna, vol. 84, no.202, pp. 112-119, jul. 2017. https://doi.org/10.15446/dyna.v84n202.63904
- arrow_upward [18] L. E. Ordóñez-Santos, J. Martínez-Girón y A. M. Figueroa-Molano, “Effect of the addition of peach palm (Bactris gasipaes) peel flour on the color and sensory properties of wheat bread”, Rev. Ciências Agrárias, vol. 39, no.3, pp. 456-462, ene. 2016. https://dx.doi.org/10.19084/RCA16008
- arrow_upward [19] aoac, Official Methods Of Analysis of aoac International, 17th Edn. Gaithersburg (Maryland): Agricultural Chemicals, contaminants, drugs AOAC, 1997. Disponible en: https://repositorioinstitucional.ceu.es/handle/10637/3158
- arrow_upward [20] Icontec. Instituto Colombiano de Normas Técnicas y Certificación. Norma Técnica Colombiana. NTC 4592, “Productos de frutas y verduras.determinación del pH”, p. 4, 1999. Disponible en: https://kupdf.net/download/ntc-4592-ph_59de20d808bbc55168e657de_pdf
- arrow_upward [21] aoc International,“Official Methods of Analysis method 936.07 Ash of Flour”, vol. 5. Gaithersburg, 1999. Disponible en: https://es.scribd.com/doc/315519697/AOAC-Official-Method-936-07-Ash-of-Flour
- arrow_upward [22] L. E. Ordóñez-Santos, J. Martínez-Girón y M. E. Arias-Jaramillo, “Effect of ultrasound treatment on visual color, vitamin C, total phenols y carotenoids content in Cape gooseberry juice”, Food Chem., vol. 233, pp. 96-100, oct. 2017. https://doi.org/10.1016/j.foodchem.2017.04.114
- arrow_upward [23] J. Martínez-Girón, X. Rodríguez-Rodríguez, L. X. Pinzón-Zárate y L. Ordóñez-Santos, “Caracterización fisicoquímica de harina de residuos del fruto de chontaduro (Bactris gasipaes Kunth, Arecaceae) obtenida por secado convectivo”, Corpoica Cienc Tecnol Agropecu., vol. 18, no.3, pp. 599-613, ago. 2017. https://doi.org/10.21930/rcta.vol18_num3_art:747
- arrow_upward [24] H. G. Cuastumal Canacuan, B. L. Valencia Murillo y L. E. Ordoñez Santos, “Efectos de los tratamientos térmicos en la concentración de vitamina C y color superficial en tres frutas tropicales”, Rev. Lasallista Investig., vol. 13, no.1, pp. 85-93, jun. 2016. https://doi.org/10.22507/rli.v13n1a7
- arrow_upward [25] C. Vasco, J. Ruales y A. Kamal-Eldin, “Total phenolic compounds and antioxidant capacities of major fruits from Ecuador”, Food Chem., vol. 111, no. 4, pp. 816-823, dic. 2008. https://doi.org/10.1016/j.foodchem.2008.04.054
- arrow_upward [26] D. Ramful, E. Tarnus, O. I. Aruoma, E. Bourdon y T. Bahorun, “Polyphenol composition, vitamin C content and antioxidant capacity of Mauritian citrus fruit pulps”, Food Res. Int., vol. 44, no. 7, pp. 2088-2099, Aug, 2011. https://doi.org/10.1016/j.foodres.2011.03.056
- arrow_upward [27] Y. Tekgül y T. Baysal, “Comparative evaluation of quality properties and volatile profiles of lemon peels subjected to different drying techniques”, J. Food Process Eng., vol. 41, no. 8, pp. 1-9, oct. 2018. https://doi.org/10.1111/jfpe.12902
- arrow_upward [28] E. Roselló-Soto et al., “Clean recovery of antioxidant compounds from plant foods, by-products and algae assisted by ultrasounds processing. Modeling approaches to optimize processing conditions”, Trends Food Sci. Technol., vol. 42, no. 2, pp. 134-149, abr. 2015. https://doi.org/10.1016/j.tifs.2015.01.002
- arrow_upward [29] N. F. A. Rahman, R. Shamsudin, A. Ismail, N. N. A. Karim Shah y J. Varith, “Effects of drying methods on total phenolic contents and antioxidant capacity of the pomelo (Citrus grandis (L.) Osbeck) peels”, Innov. Food Sci. Emerg. Technol., vol. 50, pp. 217-225, dic. 2018. https://doi.org/10.1016/j.ifset.2018.01.009
- arrow_upward [30] X. A. Ruiz-Armenta et al., “Effect of extrusion on the carotenoid content, physical and sensory properties of snacks added with bagasse of naranjita fruit: optimization process”, CyTA-J. Food, vol. 16, no.1, pp. 172-180, sep. 2017. https://doi.org/10.1080/19476337.2017.1368717
- arrow_upward [31] M. T. Pacheco, F. J. Moreno y M. Villamiel, “Chemical and physicochemical characterization of orange by‐products derived from industry”, Sci. Food Agric., vol. 99, no. 2, pp. 868-876, Jan. 2019. https://doi.org/10.1002/jsfa.9257
- arrow_upward [32] A. Cilla, L. Bosch, R. Barberá y A. Alegría, “Effect of processing on the bioaccessibility of bioactive compounds. A review focusing on carotenoids, minerals, ascorbic acid, tocopherols and polyphenols”, J. Food Compos. Anal., vol. 68, pp. 3-15, may. 2018. https://doi.org/10.1016/j.jfca.2017.01.009
- arrow_upward [33] L. Cárcamo-Medina, M. Elezar-Turcios y L. Ordóñez-Santos, “Cambios en los compuestos bioactivos del jugo de uchuva (Physalis peruviana L) pasteurizado”, TecnoLógicas, vol. 22, no.45, pp. 145-153, may. 2019. https://doi.org/10.22430/22565337.1279
- arrow_upward [34] S. Hayward, T. Cilliers y P. Swart, “Lipoxygenases: From Isolation to Application”, Compr. Rev. Food Sci. Food Saf., vol. 16, n.°1, pp. 199-211, ene. 2017. https://doi.org/10.1111/1541-4337.12239
- arrow_upward [35] A. Conesa et al., “Changes in the content of chlorophylls and carotenoids in the rind of Fino 49 lemons during maturation and their relationship with parameters from the Cielab color space”, Sci. Hortic. (Amsterdam), vol. 243, no. 3, pp. 252-260, Jan. 2019. https://doi.org/10.1016/j.scienta.2018.08.030
- arrow_upward [36] S. N. Casarotti, T. F. Borgonovi, C. L. F. M. Batista y A. L. B. Penna, “Guava, orange and passion fruit by-products: Characterization and its impacts on kinetics of acidification and properties of probiotic fermented products”, LWT, vol. 98, pp. 69-76, Dec. 2018. https://doi.org/10.1016/j.lwt.2018.08.010
- arrow_upward [37] A. Agócs, V. Nagy, Z. Szabó, L. Márk, R. Ohmacht y J. Deli, “Comparative study on the carotenoid composition of the peel and the pulp of different citrus species”, Innov. Food Sci. Emerg. Technol., vol. 8, pp. 390-394, Sep. 2007. https://doi.org/10.1016/j.ifset.2007.03.012
- arrow_upward [38] E. Vieira da Silva Júnior, L. Lins de Melo, R. A. Batista de Medeiros, Z. M. Pimenta Barros y P. M. Azoubel, “Influence of ultrasound and vacuum assisted drying on papaya quality parameters”, LWT, vol. 97, pp. 317-322, Nov. 2018. https://doi.org/10.1016/j.lwt.2018.07.017
- arrow_upward [39] C. M. Ajila, M. Aalami, K. Leelavathi, y U. J. S. Rao, “Mango peel powder: A potential source of antioxidant and dietary fiber in macaroni preparations,” Innov. Food Sci. Emerg. Technol., vol. 11, no. 1, pp. 219–224, Jan. 2010. https://doi.org/10.1016/j.ifset.2009.10.004
- arrow_upward [40] C. M. Ajila, K. Leelavathi y U. J. S. Prasada- Rao, “Improvement of dietary fiber content and antioxidant properties in soft dough biscuits with the incorporation of mango peel powder”, J. Cereal Sci., vol. 48, no. 2, pp. 319-326, Sep. 2008. https://doi.org/10.1016/j.jcs.2007.10.001
- arrow_upward [41] M. H. Azizi, J. S. Andrade, J. S. Lemos, S. J. Souza, R. S. De Souza y Z. Hadian, “Quality of wheat bread incorporated with different levels of peach palm flour (Bactris gasipaes Kunth)”, Trop. Agric. Food Sci., vol. 40, no. 1 1 pp. 13-22, 2012. Disponible en: https://pdfs.semanticscholar.org/ac2c/655cd5e3267dd5948d8ebb96e03120775b73.pdf?_ga=2.15116278.1306929556.1582052545-157729077.1571259895
- arrow_upward [42] A. Hidalgo, A. Brandolini y C. Pompei, “Carotenoids evolution during pasta, bread and water biscuit preparation from wheat flours”, Food Chem., vol. 121, no. 3, pp. 746-751, Aug. 2010. https://doi.org/10.1016/j.jcs.2010.06.002
CONTRIBUCIÓN DE LOS AUTORES
1 Investigador principal del proyecto de investigación Evaluación del potencial agroindustrial de los pigmentos carotenoides extraídos de piel de mandarina como colorante natural en productos de panificación, que permitió el desarrollo de la presente investigación; líder de la presente investigación, responsable del componente metodológico de las variables de respuesta, análisis estadístico y de la escritura del documento científico.
2 Estudiante de maestría del proyecto de investigación Evaluación del potencial agroindustrial de los pigmentos carotenoides extraídos de piel de mandarina como colorante natural en productos de panificación, que permitió el desarrollo de la presente investigación; responsable de la ejecución experimental y apoyo en la escritura del documento científico.
3 Coautor del proyecto de investigación Evaluación del potencial agroindustrial de los pigmentos carotenoides extraídos de piel de mandarina como colorante natural en productos de panificación, que permitió el desarrollo de la presente investigación; responsable del apoyo del componente metodológico, orientación en la preparación y adecuación de las muestras de estudio.
CONFLICTOS DE INTERÉS
Ningún autor tiene conflicto alguno que declarar.